
Eje corazón-intestino en la enfermedad cardiometabólica: vías mediadas por el microbioma que vinculan el síndrome metabólico con el riesgo cardiovascular
Investigadores croatas publicaron en la edición del 26 de febrero de 2026 de Medicina (de Kaunas) los resultados de una revisión sistemática que analizó el rol de la flora intestinal en el desarrollo de la enfermedad cardiometabólica*.
La NOTICIA DEL DÍA se ocupará hoy de comentar estos hallazgos.
Al inicio de su análisis, los autores señalaron que las enfermedades cardiometabólicas, término que engloba el síndrome metabólico (SM) y la enfermedad cardiovascular (ECV), representan una importante carga para la salud mundial y son las principales causas de morbilidad y mortalidad en todo el mundo.
Si bien tradicionalmente se han considerado entidades clínicas distintas, estas afecciones comparten mecanismos fisiopatológicos comunes, como la inflamación crónica de bajo grado, la resistencia a la insulina, la disfunción endotelial y la alteración del metabolismo lipídico.
En los últimos años, la microbiota intestinal ha surgido como un modulador central de estos procesos interconectados, dando lugar al concepto del eje corazón-intestino.
La microbiota intestinal humana comprende un ecosistema complejo de billones de microorganismos que interactúan dinámicamente con los sistemas metabólico, inmunitario y cardiovascular (CV) del huésped.
Los primeros estudios de referencia demostraron que la composición microbiana intestinal difiere entre individuos delgados y obesos, y que la microbiota puede influir directamente en la obtención de energía y el almacenamiento de grasa del huésped.
Estudios experimentales y en humanos posteriores establecieron aún más un papel causal de la microbiota intestinal en la regulación metabólica, mostrando que el trasplante de microbiota de donantes obesos puede inducir disfunción metabólica en receptores libres de gérmenes.
Estos hallazgos posicionaron la disbiosis intestinal como un factor clave en el desarrollo del SM.
En la diabetes mellitus tipo 2 (DM2), los estudios metagenómicos a gran escala han reportado consistentemente alteraciones específicas de la enfermedad en la composición y función de la microbiota intestinal, independientemente del trasfondo genético y la geografía.
Es importante destacar que se ha demostrado que los tratamientos farmacológicos como la metformina modifican sustancialmente el microbioma intestinal, lo que subraya la necesidad de diferenciar las firmas microbianas específicas de la enfermedad de los efectos del tratamiento.
Las revisiones que integran estos hallazgos respaldan una relación bidireccional entre el metabolismo de la glucosa y la microbiota intestinal, mediada a través de la inflamación, la señalización de ácidos biliares y los metabolitos microbianos.
Más allá de la regulación metabólica, cada vez hay más evidencia que implica a la microbiota intestinal en la patología cardiovascular.
La disbiosis se ha asociado con aterosclerosis, hipertensión e insuficiencia cardíaca a través de múltiples mecanismos interrelacionados, incluyendo la activación inmunitaria, la disfunción endotelial y la alteración de la comunicación metabólica entre el huésped y los microbios.
Una de las vías más estudiadas involucra el N-óxido de trimetilamina (TMAO) derivado de la microbiota, un metabolito producido a partir de la fosfatidilcolina y la L-carnitina de la dieta.
Los niveles elevados de TMAO circulante se han relacionado con aterosclerosis, trombosis y resultados cardiovasculares adversos tanto en estudios observacionales como mecanicistas.
Además del TMAO, se han identificado varios metabolitos emergentes derivados del intestino como posibles mediadores del riesgo cardiometabólico.
Así, se ha demostrado que la fenilacetilglutamina (PAGln) promueve la hiperreactividad plaquetaria y aumenta el riesgo cardiovascular (RCV) a través de la señalización del receptor adrenérgico.
El propionato de imidazol (ImP), un metabolito microbiano derivado de la histidina, altera la señalización de la insulina a través de la activación de mTORC1 y recientemente se ha implicado tanto en la DM2 como en la aterosclerosis.
Otros productos microbianos, incluidos los ácidos grasos de cadena corta (AGCC) y los indoles derivados del triptófano, ejercen efectos dependientes del contexto sobre la inflamación, la regulación de la presión arterial y la homeostasis metabólica.
A pesar de la creciente cantidad de literatura científica, aún no se ha sintetizado completamente hasta qué punto los mecanismos mediados por la microbiota intestinal integran la EM y la RCV dentro de un eje corazón-intestino unificado.
Las revisiones existentes suelen centrarse en entidades patológicas o metabolitos individuales, lo que limita la interpretación traslacional en todo el espectro cardiometabólico.
Por lo tanto, se justifica una síntesis exhaustiva de la evidencia en humanos que vincule la disbiosis intestinal, los metabolitos microbianos y los resultados cardiometabólicos.
Por consiguiente, esta revisión sistemática tiene como objetivo resumir la evidencia actual en humanos sobre el papel de la microbiota intestinal en las enfermedades cardiometabólicas, con especial énfasis en el síndrome metabólico como factor metabólico clave de la reactividad cardiovascular.
Mediante la integración de datos sobre la composición microbiana, las vías funcionales y los metabolitos derivados del intestino, esta revisión busca esclarecer los vínculos mecanísticos dentro del eje corazón-intestino e identificar lagunas que puedan orientar futuras estrategias preventivas y terapéuticas dirigidas al microbioma.
Reiterando lo dicho para resumir, la enfermedad cardiometabólica, término que engloba el síndrome metabólico (SM) y la enfermedad cardiovascular (ECV), representa una importante y creciente carga para la salud mundial, impulsada por la disfunción metabólica y cardiovascular interconectada.
La evidencia emergente sugiere que la microbiota intestinal desempeña un papel central en la modulación de las vías metabólicas, inflamatorias y cardiovasculares (CV), dando lugar al concepto del eje corazón-intestino.
Sin embargo, la evidencia humana que integra los mecanismos mediados por el microbioma en todo el espectro cardiometabólico aún no se ha sintetizado por completo.
Esta revisión sistemática focalizada tuvo como objetivo sintetizar la evidencia humana actual sobre los mecanismos mediados por el microbioma que vinculan el síndrome metabólico (SM) y los fenotipos metabólicos relacionados con el riesgo cardiovascular (RCV) y los resultados cardiovasculares (CV) subclínicos dentro del marco conceptual del eje corazón-intestino.
A tales fines se realizó una búsqueda sistemática de la literatura en PubMed, Scopus, Web of Science y la Biblioteca Cochrane de acuerdo con las guías PRISMA 2020.
Se incluyeron estudios observacionales e intervencionistas en humanos que evaluaban la composición, la función o los metabolitos derivados de la microbiota intestinal en relación con los resultados cardiometabólicos y cardiovasculares.
El riesgo de sesgo se evaluó utilizando las herramientas Cochrane RoB 2 y ROBINS-I, y los hallazgos se sintetizaron de forma narrativa.
Diez estudios en humanos publicados entre 2016 y 2025 cumplieron los criterios de inclusión.
En todos estos estudios, la disbiosis intestinal se asoció consistentemente con perfiles de riesgo cardiometabólico adversos y resultados cardiovasculares subclínicos, incluyendo resistencia a la insulina, inflamación sistémica, aterosclerosis subclínica y pronóstico cardiovascular en poblaciones de alto riesgo.
Los metabolitos derivados de la microbiota, en particular el N-óxido de trimetilamina (TMAO) y los ácidos grasos de cadena corta (AGCC), así como metabolitos emergentes como la fenilacetilglutamina (PAGln) y el propionato de imidazol (ImP), se identificaron como mediadores clave que vinculan el síndrome metabólico y las alteraciones metabólicas relacionadas con la reactividad cardiovascular (RCV) y la enfermedad cardiovascular (ECV) subclínica.
Los marcadores de disfunción de la barrera intestinal y la endotoxemia respaldaron aún más el papel de la inflamación crónica de bajo grado dentro del eje corazón-intestino.
Al proponer el debate acerca de las observaciones realizadas, los autores propusieron varios ejes temáticos:
1. El eje corazón-intestino como marco cardiometabólico integrador
Los hallazgos de esta revisión sistemática respaldan el eje corazón-intestino como un marco biológico integrador que vincula el síndrome metabólico con el riesgo cardiovascular.
En los estudios en humanos incluidos, las alteraciones en la composición, el potencial funcional y la producción de metabolitos de la microbiota intestinal se asociaron consistentemente con fenotipos metabólicos y cardiovasculares adversos.
Estas observaciones refuerzan el concepto de que la disbiosis intestinal actúa como un amplificador de las vías de riesgo cardiometabólico ya establecidas, en lugar de ser un factor aislado o independiente en el desarrollo de la enfermedad.
Este marco integrador es consistente con la evidencia mecanicista y clínica previa que identifica la microbiota intestinal como una interfaz clave entre las exposiciones ambientales y la regulación cardiometabólica del huésped.
Se ha demostrado que las interacciones dieta-microbiota, las terapias farmacológicas y los factores del estilo de vida modulan el metabolismo del huésped y la CVR a través de mecanismos dependientes del microbioma.
En conjunto, estos datos respaldan el eje corazón-intestino como una construcción dinámica a nivel de sistemas en lugar de una vía unidireccional.
Para facilitar la integración conceptual, se proporciona un resumen gráfico del eje corazón-intestino propuesto en la figura (ver).
El esquema ilustra la disfunción relacionada con el síndrome metabólico como un amplificador inicial de la disbiosis intestinal y la actividad metabólica derivada del microbioma, destacando nodos mecanísticos clave, incluidos los metabolitos microbianos, la disfunción de la barrera intestinal con endotoxemia y la inflamación crónica de bajo grado, y sus consecuencias cardiometabólicas posteriores, como la resistencia a la insulina, la disfunción endotelial, la aterosclerosis subclínica y el pronóstico cardiovascular adverso.
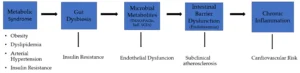
Figura. Representación esquemática del eje corazón-intestino que ilustra el síndrome metabólico como un factor que amplifica la disbiosis intestinal, los metabolitos derivados de la microbiota, la disfunción de la barrera intestinal y la inflamación crónica de bajo grado. Estas vías interconectadas contribuyen a la resistencia a la insulina, la disfunción endotelial, la aterosclerosis subclínica y el aumento del riesgo cardiovascular.
2. El síndrome metabólico como factor clave en las interacciones entre el microbioma y el sistema cardiovascular.
El síndrome metabólico surgió como un factor clave que moldea las interacciones entre el microbioma y el CV en los estudios incluidos.
Ambas afecciones se caracterizan por resistencia a la insulina, inflamación crónica de bajo grado y alteración de la ecología microbiana intestinal, lo que crea un entorno metabólico que puede aumentar la susceptibilidad del huésped a las señales derivadas del microbioma.
Estudios metagenómicos a gran escala han demostrado alteraciones específicas de la enfermedad en la diversidad microbiana y las vías funcionales en el síndrome metabólico, hallazgos que también están respaldados por análisis de microbioma basados en la población.
Es importante destacar que la resistencia a la insulina representa un vínculo mecanicista clave entre la enfermedad metabólica y la patología cardiovascular.
Varios estudios incluidos sugieren que los estados de enfermedad metabólica sensibilizan el sistema cardiovascular a los metabolitos derivados del intestino y a los mediadores inflamatorios.
Por ejemplo, la disbiosis de la microbiota intestinal se asoció con un pronóstico cardiovascular adverso en pacientes con enfermedad coronaria y diabetes tipo 2, mientras que distintos perfiles microbianos se vincularon con la enfermedad cardiovascular subclínica en individuos con diabetes tipo 2.
Estas observaciones coinciden con datos experimentales que demuestran que las interacciones entre la microbiota y los lípidos pueden exacerbar la inflamación del tejido adiposo a través de vías de señalización inmune innata.
3. Metabolitos derivados de la microbiota: más allá del N-óxido de trimetilamina
Los metabolitos derivados de la microbiota representan un vínculo mecanístico central dentro del eje corazón-intestino.
El TMAO sigue siendo el metabolito más estudiado, y los estudios de cohortes humanas asocian consistentemente niveles elevados de TMAO circulante con aterosclerosis subclínica, incidencia de ECV y pronóstico adverso.
En pacientes con insuficiencia cardíaca, los niveles elevados de TMAO también se han relacionado con peores resultados clínicos, lo que subraya su relevancia en todo el espectro de la ECV.
Sin embargo, centrarse exclusivamente en el TMAO puede simplificar en exceso la complejidad de las interacciones entre el microbioma y el riesgo cardiometabólico.
Se ha demostrado que la PAGln promueve la hiperreactividad plaquetaria y aumenta el riesgo cardiovascular a través de la señalización del receptor adrenérgico.
El ImP, un metabolito microbiano derivado de la histidina, altera la señalización de la insulina mediante la activación de mTORC1 y recientemente se ha implicado tanto en la diabetes tipo 2 como en la aterosclerosis.
En conjunto, estos hallazgos sugieren que el riesgo cardiometabólico está determinado por una red de metabolitos microbianos que interactúan entre sí, en lugar de una única vía dominante.
4. Disfunción de la barrera intestinal, endotoxemia e inflamación sistémica
La alteración de la integridad de la barrera intestinal constituye un mecanismo clave adicional que vincula la disbiosis intestinal con la enfermedad cardiometabólica.
Varios de los estudios incluidos evaluaron marcadores de aumento de la permeabilidad intestinal y endotoxemia metabólica, lo que respalda el concepto de que la translocación de componentes microbianos a la circulación sistémica contribuye a la inflamación crónica de bajo grado.
Cabe destacar que la modulación de la microbiota intestinal se asoció con reducciones en los niveles de proteína de unión a LPS (lipopolisacáridos) y marcadores inflamatorios sistémicos en individuos con sobrepeso y obesidad.
Este entorno inflamatorio es un factor determinante reconocido de la resistencia a la insulina, la disfunción endotelial y la aterosclerosis.
Los datos experimentales y clínicos también respaldan el papel de la disfunción de la barrera intestinal como un factor permisivo que amplifica los efectos metabólicos y vasculares posteriores de los metabolitos derivados de la microbiota.
Dentro del eje corazón-intestino, la integridad intestinal deteriorada puede, por lo tanto, actuar sinérgicamente con la actividad metabólica microbiana para promover la progresión de la enfermedad cardiometabólica.
5. Efectos dependientes del contexto de los ácidos grasos de cadena corta y los metabolitos del indol
Los AGCC ejemplifican la naturaleza dependiente del contexto de los efectos cardiometabólicos mediados por el microbioma.
Tanto en modelos experimentales como en estudios en humanos, los AGCC se han asociado con una mejor sensibilidad a la insulina, metabolismo lipídico y regulación de la presión arterial.
La evidencia emergente sugiere además que la detección de AGCC por parte del huésped a través de receptores acoplados a proteínas G puede ejercer efectos protectores contra la hipertensión.
En los estudios incluidos, los perfiles de AGCC fecales reflejaron una disbiosis cardiometabólica subyacente y se asociaron con obesidad e hipertensión, mientras que las intervenciones dietéticas modularon favorablemente los patrones de AGCC en paralelo con mejoras en los marcadores de riesgo metabólico.
De manera similar, los metabolitos indólicos derivados del triptófano, en particular el ácido indolpropiónico, se han asociado con un menor riesgo de DM2 y complicaciones metabólicas relacionadas, y una menor inflamación sistémica.
En conjunto, estos hallazgos subrayan los roles duales y dependientes del contexto de los metabolitos derivados del microbioma dentro del eje corazón-intestino.
6. Implicancias clínicas y potencial traslacional
El creciente reconocimiento del eje corazón-intestino tiene importantes implicancias clínicas.
Las intervenciones dirigidas al microbioma, incluyendo la modificación dietética, los probióticos, el trasplante de microbiota fecal y las terapias microbianas de nueva generación, han demostrado potencial para mejorar los parámetros metabólicos en poblaciones seleccionadas.
En los estudios de intervención incluidos en esta revisión, la modulación dirigida de la microbiota intestinal mejoró la sensibilidad a la insulina, los perfiles lipídicos y los marcadores de riesgo cardiometabólico.
La evidencia humana disponible abarca diseños de estudio heterogéneos, incluyendo ensayos de intervención aleatorizados, cohortes prospectivas y análisis transversales, con resultados cardiovasculares predominantemente marcadores metabólicos e inflamatorios y fenotipos cardiovasculares subclínicos en lugar de criterios de valoración clínicos duros.
Sin embargo, la variabilidad interindividual en la composición del microbioma y la respuesta del huésped sigue siendo sustancial.
Por lo tanto, podrían ser necesarias intervenciones nutricionales personalizadas e informadas sobre el microbioma para lograr beneficios cardiometabólicos clínicamente significativos.
En la actualidad, la evidencia que respalda la reducción directa del riesgo cardiovascular mediante intervenciones basadas en el microbioma sigue siendo limitada, lo que subraya la necesidad de una traslación clínica cautelosa.
Es importante destacar que las implicancias clínicas aquí discutidas deben interpretarse principalmente como generadoras de hipótesis.
La mayoría de los estudios incluidos son de naturaleza observacional y se basan en resultados cardiovasculares indirectos o subclínicos, con una relativa escasez de datos sobre resultados cardiovasculares directos.
Por lo tanto, las estrategias dirigidas al microbioma deben considerarse actualmente como vías de investigación complementarias en lugar de intervenciones terapéuticas establecidas para la reducción del riesgo cardiovascular.
7. Consideraciones metodológicas y futuras líneas de investigación
Una consideración metodológica importante para interpretar la evidencia humana disponible es la considerable heterogeneidad entre los estudios incluidos.
Las diferencias en las técnicas de secuenciación del microbioma (secuenciación del gen ARNr 16S frente a metagenómica de escopeta), los flujos de trabajo bioinformáticos, las exposiciones dietéticas, el uso de medicamentos y las características de la población limitan la comparabilidad directa e impiden una síntesis cuantitativa significativa.
En lugar de intentar agregar estadísticamente datos heterogéneos, esta revisión adoptó un enfoque narrativo orientado a los mecanismos para contextualizar los hallazgos dentro del marco del eje corazón-intestino.
Esta heterogeneidad se extiende no solo a los métodos de evaluación del microbioma, sino también al diseño del estudio, los perfiles de riesgo de la población y la naturaleza de los resultados cardiometabólicos y cardiovasculares evaluados.
Es importante destacar que la heterogeneidad no se consideró únicamente una limitación, sino una característica inherente a la investigación del microbioma humano que influye en la selección e interpretación de los estudios.
Al priorizar los estudios con una caracterización suficiente del microbioma y criterios de valoración cardiometabólicos o cardiovasculares clínicamente interpretables, el diseño focalizado buscó preservar la interpretabilidad mecanicista, al tiempo que reconocía la variabilidad entre los diseños de estudio y las poblaciones.
Diversas consideraciones metodológicas merecen un análisis detallado.
El número de estudios en humanos que cumplen los criterios de inclusión sigue siendo limitado, y se observa una heterogeneidad considerable en los diseños de estudio, las técnicas de evaluación del microbioma, los flujos de trabajo analíticos y los resultados cardiometabólicos notificados.
La variabilidad en las plataformas de secuenciación, los flujos de trabajo bioinformáticos y los métodos de cuantificación de metabolitos dificulta la comparabilidad directa entre estudios y limita la capacidad de obtener conclusiones cuantitativas sólidas.
Además, resulta difícil tener en cuenta por completo factores de confusión como los patrones dietéticos, el uso de medicamentos y los hábitos de vida, especialmente en los estudios observacionales, y estos pueden influir sustancialmente tanto en la composición del microbioma como en los fenotipos cardiometabólicos.
Por lo tanto, la investigación futura debería priorizar estudios humanos longitudinales e intervencionistas bien diseñados que integren el perfilado estandarizado del microbioma con enfoques multiómicos complementarios, incluyendo la metabolómica, junto con imágenes cardiovasculares y criterios de valoración clínicos sólidos.
La armonización de los enfoques metodológicos y los estándares de presentación de informes será fundamental para mejorar la reproducibilidad y la comparabilidad entre estudios.
La aplicación de marcos metodológicos validados y herramientas de evaluación de la calidad fortalecerá aún más la inferencia causal y mejorará la relevancia traslacional de los hallazgos basados en el microbioma dentro del campo cardiometabólico.
En consecuencia, algunas conclusiones mecanicistas en esta revisión se derivan principalmente de cohortes más pequeñas o exploratorias, mientras que las asociaciones que involucran metabolitos clave derivados de la microbiota y fenotipos cardiovasculares subclínicos están respaldadas por estudios de cohortes más grandes o hallazgos más consistentes en poblaciones independientes.
Esta distinción debe considerarse al interpretar la fuerza relativa de la evidencia humana disponible.
Las evaluaciones del riesgo de sesgo informaron aún más la interpretación de los hallazgos en lugar de servir como criterios de exclusión.
Los estudios de intervención se caracterizaron generalmente por un bajo riesgo de sesgo o algunas limitaciones, mientras que los estudios observacionales mostraron predominantemente un riesgo moderado de sesgo, debido principalmente a factores de confusión residuales y a la selección de participantes.
Estas diferencias se tuvieron en cuenta al interpretar la solidez de la evidencia, en particular para las asociaciones entre las características de la microbiota intestinal y los resultados cardiovasculares.
A diferencia de revisiones anteriores que suelen centrarse en componentes aislados del eje intestino-corazón —como metabolitos individuales, estados patológicos específicos o evidencia preclínica—, la presente revisión ofrece una síntesis integrada, basada en evidencia humana, de los mecanismos mediados por el microbioma que vinculan el síndrome metabólico con la reactividad cardiovascular.
Una contribución conceptual clave es la definición explícita del síndrome metabólico como un estado metabólico amplificador que aumenta la susceptibilidad del huésped a las señales derivadas del microbioma, en lugar de como una condición paralela o independiente.
Además, esta revisión integra de forma única la composición microbiana intestinal, la capacidad funcional, los metabolitos microbianos (incluidos TMAO, AGCC, PAGln e ImP), la disfunción de la barrera intestinal y la inflamación crónica de bajo grado en un modelo mecanicista multicapa unificado, basado exclusivamente en estudios en humanos.
Al consolidar estas vías interconectadas, la revisión ofrece un marco traslacional más claro para comprender cómo la disfunción metabólica interactúa con la patología cardiovascular dentro del eje corazón-intestino.
La presente revisión sistemática tiene varias limitaciones que deben reconocerse.
En primer lugar, el número de estudios en humanos elegibles fue relativamente limitado, lo que refleja la naturaleza incipiente de la investigación sobre el eje corazón-intestino en la enfermedad cardiometabólica.
El número limitado de estudios elegibles debe interpretarse en el contexto de los estrictos criterios de inclusión aplicados.
Solo se incluyeron estudios con una caracterización adecuada del microbioma y resultados cardiometabólicos o cardiovasculares clínicamente interpretables, lo que redujo la heterogeneidad, pero necesariamente limitó el tamaño de la base de evidencia final.
Esta compensación se consideró apropiada para respaldar una síntesis mecanicista significativa en lugar de una agregación descriptiva amplia.
Además, se observó una heterogeneidad sustancial entre los estudios incluidos en términos de diseño del estudio, características de la población, técnicas de evaluación del microbioma y resultados cardiometabólicos y cardiovasculares informados, lo que limita la comparabilidad directa.
En segundo lugar, una proporción sustancial de la evidencia disponible fue observacional, lo que restringe la inferencia causal.
Aunque se incluyeron estudios de intervención, los tamaños de muestra fueron generalmente modestos y las duraciones de seguimiento fueron relativamente cortas.
En tercer lugar, la variabilidad en los métodos de perfilado del microbioma y el enfoque en taxones microbianos seleccionados o metabolitos predefinidos pueden no reflejar completamente la complejidad de las vías cardiometabólicas impulsadas por el microbioma.
Además, la solidez del la inferencia mecanicista varía entre los estudios incluidos.
Algunas conclusiones de esta revisión se derivan principalmente de cohortes más pequeñas o exploratorias, mientras que las asociaciones que involucran metabolitos clave derivados de la microbiota y fenotipos cardiovasculares subclínicos están respaldadas por cohortes más grandes o hallazgos más consistentes en poblaciones independientes.
Esta distinción debe considerarse al interpretar la robustez relativa de las vías individuales dentro del eje corazón-intestino.
A pesar de estas limitaciones, los estudios incluidos proporcionan valiosa evidencia humana que respalda los mecanismos mediados por el microbioma que vinculan el síndrome metabólico con la reactividad cardiovascular dentro del marco del eje corazón-intestino.
Como conclusiones, esta revisión sistemática sintetiza la evidencia actual en humanos que respalda el eje corazón-intestino como un marco biológicamente plausible y clínicamente relevante que vincula el síndrome metabólico (SM) con la reactividad cardiovascular (RCV).
Tanto en estudios observacionales como intervencionistas, se observaron asociaciones consistentes entre la disbiosis intestinal, los metabolitos derivados de la microbiota, la disfunción de la barrera intestinal y los resultados cardiometabólicos y cardiovasculares adversos.
En conjunto, estos hallazgos posicionan a la microbiota intestinal como un modulador activo de la progresión de la enfermedad cardiometabólica, en lugar de un mero espectador pasivo.
Es importante destacar que esta revisión resalta el SM y las alteraciones metabólicas relacionadas como estados centrales que pueden amplificar la susceptibilidad del huésped a las señales derivadas del microbioma.
Los metabolitos microbianos como el TMAO y los ácidos grasos de cadena corta (AGCC), junto con compuestos emergentes como la PAGln y el ImP, parecen operar dentro de vías metabólicas, inflamatorias y vasculares interconectadas que vinculan la disfunción intestinal con la patología cardiovascular.
Paralelamente, la evidencia que implica el deterioro de la barrera intestinal y la endotoxemia de bajo grado en la inflamación sistémica respalda aún más un modelo mecanicista multicapa del eje corazón-intestino.
Desde una perspectiva clínica, los datos disponibles en humanos sugieren que las intervenciones dirigidas al microbioma, en particular la modulación dietética y las estrategias con probióticos seleccionados, pueden influir favorablemente en los perfiles de riesgo cardiometabólico.
Sin embargo, la evidencia de reducciones directas en el riesgo cardiovascular sigue siendo limitada, y la considerable variabilidad interindividual en la composición basal del microbioma y la respuesta al tratamiento continúa representando un desafío importante para la traslación clínica.
Estas observaciones subrayan la necesidad de enfoques personalizados y dependientes del contexto, en lugar de intervenciones uniformes y estandarizadas basadas en el microbioma.
La investigación futura debería priorizar estudios longitudinales y de intervención en humanos bien diseñados que integren la caracterización estandarizada del microbioma con la metabolómica, las imágenes cardiovasculares y los resultados clínicos objetivos.
Estos enfoques integradores serán esenciales para fortalecer la inferencia causal, identificar biomarcadores microbianos o metabólicos robustos del riesgo cardiovascular y definir las poblaciones de pacientes con mayor probabilidad de beneficiarse de estrategias preventivas o terapéuticas basadas en el microbioma.
Actualmente, el principal valor del eje corazón-intestino reside en su función como marco mecanicista y generador de hipótesis, más que como base para la estratificación inmediata del riesgo clínico o la toma de decisiones terapéuticas.
En conclusión, el eje corazón-intestino representa un marco conceptual y traslacional prometedor para comprender la compleja interacción entre la disfunción metabólica y la reactividad cardiovascular.
Los avances continuos en este campo podrían, en última instancia, complementar las estrategias de prevención cardiometabólica ya establecidas y contribuir a enfoques más integrados y basados en mecanismos para la salud cardiovascular.
Palabras clave: microbiota intestinal ; eje corazón-intestino ; enfermedad cardiometabólica ; síndrome metabólico ; riesgo cardiovascular ; disbiosis ; metabolitos microbianos ; N-óxido de trimetilamina
* Bečić T, Jukić I, Prižmić PŠ, Matulić I, Đogaš H, Radić M, Radić J, Vuković J, Fabijanić D. Heart-Gut Axis in Cardiometabolic Disease: Microbiome-Mediated Pathways Linking Metabolic Syndrome to Cardiovascular Risk. Medicina (Kaunas). 2026 Feb 26;62(3):444. doi: 10.3390/medicina62030444. PMID: 41901529; PMCID: PMC13027942.








